오름테라퓨틱이 회사 핵심 신약 후보물질의 개발을 포기했다.
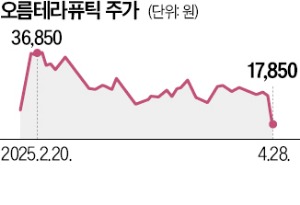
오름테라퓨틱은 인간표피성장인자수용체(HER)2 양성 유방암 등 HER2 과발현 고형암을 치료하는 신약 ‘ORM-5029’의 미국 임상 1상을 자진 중단한다고 28일 공시했다. ORM-5029는 오름테라퓨틱이 보유한 신약 후보물질군 중 가장 개발이 앞선 선도물질이었다. 그러나 지난해 11월 미국 임상에서 환자 한 명이 사망하는 중대한 이상 사례가 발생했다. 이후 회사는 신규 임상 참여자 모집을 중단했다.
당초 오름테라퓨틱은 올해 하반기 미국식품의약국(FDA)과 협의를 거쳐 임상 재개 여부를 결정할 예정이었다. 회사 측은 “환자의 안전과 제한된 임상 예산을 고려해 신속하게 결정을 내렸다”고 말했다.
ORM-5029는 오름테라퓨틱이 세계 최초로 개발한 플랫폼 항체접합분해제(DAC)로 제작했다. DAC는 항체약물접합체(ADC)의 일종이다. ADC는 타깃을 찾아가는 항체, 암세포를 죽이는 독성물질인 페이로드, 항체와 페이로드를 연결해 주는 링커로 구성된다. DAC는 페이로드로 독성물질이 아니라 표적단백질분해(TPD)를 결합했다.
현재 임상 단계인 오름테라퓨틱의 또 다른 물질은 미국 BMS에 기술이전한 골수성 백혈병(AML) 및 고위험 골수형성이상증후군 치료제 ORM-6151이다. BMS는 미국 임상 1상을 진행 중이다.
일각에서는 ORM-5029 임상 중단이 DAC 플랫폼 자체의 문제일 것이라는 우려를 제기하고 있다. 이에 회사 관계자는 “ORM-5029는 DAC 플랫폼이 아닌 링커와 항체 결합 부문에서 문제가 발생한 것으로 본다”며 “현재 해당 항체와 링커를 사용하는 물질은 더 이상 개발하고 있지 않다”고 말했다. 그는 “ORM-5029와 동일한 페이로드를 사용하되, 항체와 링커를 교체한 혈액암 신약 ORM-1153은 영장류 비임상에서 부작용이 나타나지 않았다”고 덧붙였다.
김유림 기자 youforest@hankyung.com

 6 hours ago
2
6 hours ago
2










 English (US) ·
English (US) ·