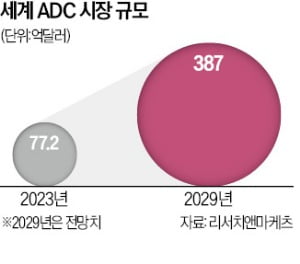
항체약물접합체(ADC) 시장 1위인 일본 다이이찌산쿄가 영국 아스트라제네카와 함께 두 번째 ADC를 승인받았다. 국내에선 리가켐바이오사이언스가 미국 제약사 얀센과 함께 유사 계열의 신약을 개발하고 있다.
다이이찌산쿄와 아스트라제네카는 유방암 ADC 신약 ‘다트로웨이’를 미국 식품의약국(FDA)으로부터 시판 허가받았다고 20일 밝혔다. 일본에선 지난해 말 승인받았다.
FDA는 이 약을 특정 유전변이(호르몬 수용체 양성, HER2 음성)가 있는 유방암 환자에게 쓸 수 있도록 허용했다. 다이이찌산쿄는 미국에 있는 일선 의료기관에서 2주 뒤부터 이 약을 처방할 수 있을 것으로 내다봤다. 약값은 월평균 4000만원 정도로 전해졌다.
한국 승인 일정은 아직 알려지지 않았다. 업체 관계자는 “지난해 하반기 한국 식품의약품안전처에 허가 신청을 한 뒤 결과를 기다리고 있다”고 말했다.
ADC는 암세포를 찾아가는 항체에 독성이 강한 약물을 붙인 항암 신약이다. 유도탄처럼 암세포만 찾아가 공격해 ‘마법의 탄환’으로 불린다. 다이이찌산쿄와 아스트라제네카는 세계 1위 ADC 신약인 ‘엔허투’를 보유하고 있다. 엔허투는 2019년 유방암에 쓰도록 FDA 승인을 받은 뒤 4년 만인 2023년 연 매출 3조원을 넘었다. 첫 허가 후 치료 가능한 질환군을 확대하면서 폐암 위암 등 다양한 암 치료에 이 약을 쓸 수 있다.
앞서 미국 길리어드가 TROP2 표적 ADC인 트로델비를 2021년 출시했지만 아직 기대할 만한 성과는 내지 못하고 있다. 치료 대상을 폐암 등으로 늘리기 위한 후속 연구에 잇따라 실패하면서다.
다이이찌산쿄와 아스트라제네카는 ‘추격자’인 다트로웨이 시장을 넓히기 위해 폐암 등 20여 개 임상시험을 하고 있다. 연 매출 목표는 7조원에 이른다. 다만 다트로웨이도 약효 면에서 기존 화학항암제보다 압도적으로 생존율을 높이지 못한 것은 한계다. 후발 주자의 진입 가능성이 아직 남아 있다는 의미다.
국내 바이오 기업 리가켐바이오는 이들을 맹추격하고 있다. 2023년 TROP2 표적 ADC 후보물질인 ‘LCB84’ 기술을 얀센에 2조2400억원 규모로 기술이전했다. 임상 1상 단계다. 미국 머크(MSD)는 중국 켈룬바이오텍이 보유한 TROP2 표적 ADC 후보물질을 도입해 공동개발하고 있다. 켈룬은 지난해 말 중국에서 해당 약의 시판 허가를 받았다.
이지현/이영애 기자 bluesky@hankyung.com

 13 hours ago
4
13 hours ago
4




![1월 둘째 주, 마켓PRO 핫종목·주요 이슈 5분 완벽정리 [위클리 리뷰]](https://img.hankyung.com/photo/202501/99.34900612.1.jpg)
!["이러다, 다 죽어!"…'오징어게임2' 망하면 큰일 난다는데 [김소연의 엔터비즈]](https://img.hankyung.com/photo/202412/01.39034730.1.jpg)
!["나랑 XX 할래"…돌봄 로봇과 성적 대화 하는 노인들 [유지희의 ITMI]](https://img.hankyung.com/photo/202501/01.39164747.1.png)






 English (US) ·
English (US) ·